Avance en terapia OpRegen de células madre para DMAE seca
Nuevo avance en terapia OPREGEN de células madre para DMAE seca.
BioTime presenta datos actualizados de prueba de fase I/IIa de OpRegen®
- No hubo eventos adversos graves relacionados con el tratamiento después de 15 meses.
- Los signos de injerto y la supervivencia celular se han mantenido.
BioTime, Inc., una compañía biotecnología de ensayos clínicos de fases avanzadas centrada en el desarrollo y comercialización de productos que abordan las enfermedades degenerativas, anunció que presentaba en la convención anual de la Academia Americana de Oftalmología (AAO) en Nueva Orleans, Louisiana, un resumen relacionado con uno de sus principales programas, OpRegen®, para la degeneración macular asociada con la edad seca (DMAE seca).
El Dr. Eyal Banin (Centro Médico de la Universidad Hebrea de Hadassah, Jerusalén, Israel), uno de los investigadores principales que participaron en el estudio, presentó los datos del estudio en curso, abierto, de aumento de dosis.
El resumen presentado se tituló, «Estudio de fase 1 y 2a de células madre humanas derivadas de células epiteliales del pigmento retinal trasplantadas subretinianamente en pacientes con degeneración macular avanzada relacionada con la edad en su forma seca«.
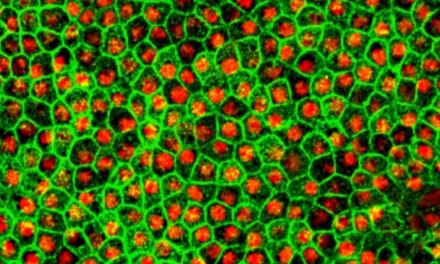
OpRegen® se compone de células del epitelio pigmentario de la retina diferenciadas derivadas de células madre humanas en estado xeno-libre.
Las observaciones del estudio abierto FaseI/IIa en curso y los resultados hasta la fecha muestran que tanto el procedimiento quirúrgico utilizado para inyectar las células OpRegen®, como OpRegen®, fueron bien tolerados.
OpRegen® mostró una seguridad continuada a largo plazo durante 15 meses y hasta la fecha no hubo eventos adversos graves sistémicos relacionados con el tratamiento.
Además de la seguridad y la tolerancia, las imágenes sugieren signos de injerto y supervivencia celular.
«Creemos que la administración de las células OpRegen®puede llegar a ser una opción terapéutica potencial para las personas con DMAE seca y actualmente estamos incluyendo de forma activa personas adicionales para comprender mejor la posibilidad que representa para estos pacientes», comentó el Dr. Eyal Banin.
OpRegen®, que está siendo estudiado para el tratamiento de la forma seca de la degeneración macular asociada a la edad (DMAE), se compone de una suspensión de células que se liberan subretinianamente durante una sola inyección intraocular.
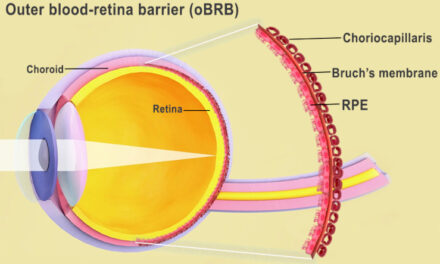
Las células del epitelio pigmentario de la retina (EPR) son componentes esenciales del revestimiento posterior de la retina y funcionan para ayudar a nutrir la retina, incluidos los fotorreceptores.
Un proceso patentado que impulsa la diferenciación de las células madre pluripotentes se utiliza para generar células del EPR de alta pureza OpRegen®.
Las células del ERP, OpRegen®, también son «xeno-libres», lo que significa que no se utilizan productos animales en ningún momento del proceso de derivación y producción.
La exclusión del uso de productos animales elimina algunas preocupaciones potenciales de seguridad.
Los estudios preclínicos en ratas han demostrado que después de un inyección subretinal única de OpRegen®, las células pueden organizarse rápidamente en su estructura monocapa natural en el espacio subretiniano y sobrevivir durante toda la vida del animal.
OpRegen® está diseñado para ser un producto “estándar” alogénico (para cualquier paciente).
A diferencia de los tratamientos que requieren múltiples inyecciones frecuentes en el ojo, se espera que OpRegen® sea administrado en una única sesión.
OpRegen® recibió la designación Fast Track (tramitación rápida) de la FDA, que permite interacciones más frecuentes con la agencia, y la elegibilidad para la aprobación acelerada y la revisión de prioridad.
OpRegen ® es una marca registrada de Cell Cure Neurosciences Ltd., una subsidiaria de propiedad mayoritaria de BioTime, Inc.