ProQR informa de la administración de la primera dosis a un paciente del ensayo STELLAR de QR-421a de fase 1/2 para el síndrome de Usher2.
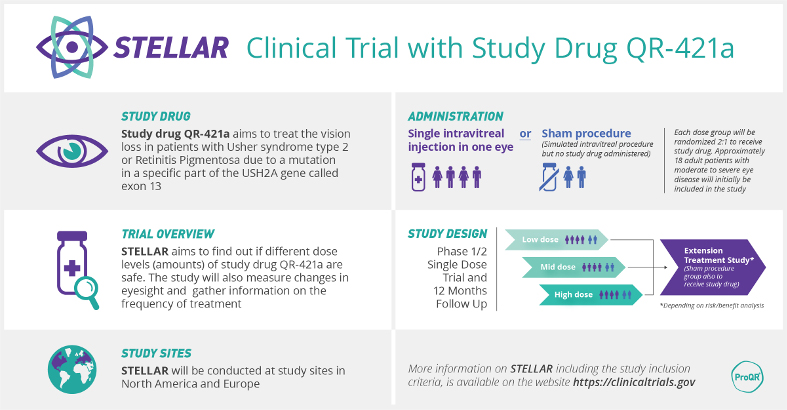
ProQR Therapeutics anunció que un primer paciente del ensayo clínico en fase 1/2 STELLAR ha recibido una dosis de QR-421a para pacientes con síndrome de Usher tipo 2 o retinosis pigmentaria no sindrómica (PR). Se espera que los datos provisionales del estudio se anuncien a mediados de 2019.
El síndrome de Usher es una degeneración retiniana hereditaria que afecta la audición, el equilibrio y la visión. El síndrome de Usher causado por mutaciones del gen USH2A es una de las causas más comunes de retinosis pigmentaria (RP) con características sindrómicas. Actualmente no hay tratamiento para los déficits sensoriales causados por el síndrome de Usher.
«No hay tratamientos efectivos para la mayoría de las enfermedades retinianas hereditarias, incluido el síndrome de Usher, y suele provocar ceguera», dijo David G. Birch, PhD, Investigador Principal de STELLAR y Director Científico de la Retina Foundation of the Southwest en Dallas, Texas.
“El estudio STELLAR es uno de los primeros estudios de este tipo que explora el impacto de las terapias ARN de ProQR en pacientes con síndrome de Usher debido a una mutación en el Exón 13. El ensayo STELLAR explorará si QR-421a (terapia de ARN de ProQR) puede retardar la progresión de la enfermedad o incluso revertirla. «Tratamientos como este, que se dirigen a la causa subyacente de un trastorno, tienen la capacidad de dar nuevas esperanzas a los pacientes y a sus familias de que las terapias que les pueden cambiar la vida podrían estar disponibles en un futuro cercano».
«El síndrome de Usher es una enfermedad devastadora, por lo que nos complace llevar el QR-421a a la clínica con el objetivo de impulsar un cambio para estos pacientes, similar a los primeros datos iniciales, pero prometedores, de sepofarsen en pacientes con LCA10«, dijo Daniel A. de Boer, director ejecutivo de ProQR, en un comunicado de prensa de la compañía. «Estamos comprometidos en avanzar rápidamente con nuestras prometedoras terapias de ARN para enfermedades hereditarias de la retina y creemos que nuestra plataforma de generación de terapias dirigidas de ARN con una duración muy prolongada en la retina y con la capacidad de llegar a la retina central y periférica, podremos dirigirnos a muchas de estas enfermedades en los próximos años».
El síndrome de Usher es la causa principal de sordera y ceguera combinadas. Las mutaciones en el exón 13 en el gen USH2A, diana para el QR-421a, causan pérdida de visión en aproximadamente 16,000 individuos en el mundo occidental.
Acerca del ensayo Phase 1/2 STELLAR
STELLAR, o PQ-421a-001, es un primer estudio en humanos que inicialmente incluirá a aproximadamente 18 adultos que tienen pérdida de visión debido a mutaciones en el exón 13 del gen USH2A y se llevará a cabo en unos siete centros especializados en América del Norte y Europa. Será un estudio aleatorizado con doble máscara que explorará varios niveles de dosis y un control (inyección simulada), administrado como una inyección intravítrea única de QR-421a en un ojo. El primer paciente en cada nivel de dosis se administrará de manera abierta. Los objetivos del ensayo incluirán la evaluación de la seguridad, la tolerabilidad, la farmacocinética y la eficacia, según lo determinado por la detención de la progresión o la mejora de la función visual y la estructura retiniana a través de puntos finales oftálmicos como el campo visual, la agudeza visual y la tomografía de coherencia óptica. Los cambios en la calidad de vida en los sujetos de prueba también serán evaluados.
Se esperan datos preliminares del primer estudio en humanos a mediados de 2019. Los pacientes que completen este ensayo podrán participar en un estudio de extensión si son elegibles. De los resultados de la prueba de dosis única se informará en la próxima fase que potencialmente incluirá una prueba controlada, adaptiva y multidosis, cuyos resultados se esperan para el 2021.
Acerca de QR-421a
QR-421a es un oligonucleótido basado en ARN de primera investigación diseñado para abordar la causa subyacente de la pérdida de visión en el síndrome de Usher tipo 2 y la retinosis pigmentaria no sindrómica (RP) debido a mutaciones en el exón 13 del gen USH2A . El QR-421a está diseñado para restaurar la proteína Usherin funcional mediante el uso de un enfoque de omisión de exón con el objetivo de detener o revertir la pérdida de visión en los pacientes. El QR-421a está destinado a ser administrado a través de inyecciones intravítreas en el ojo y se le ha otorgado la designación de medicamento huérfano en los Estados Unidos y la Unión Europea y recibió la designación de vía rápida de la FDA.
El estudio en humanos de QR-421a (PQ-421a-001) evaluará la seguridad y la tolerabilidad de una dosis única de QR-421a en sujetos adultos con RP debido a mutaciones en el exón 13 del gen USH2A.
QR-421a se administrará mediante inyección intravítrea en el peor de los ojos. También se investigará la posible relación dosis-respuesta y la duración del efecto después de una dosis única de QR-421a, basada en mejoras en la estructura retiniana o la función visual, para informar la selección del nivel de dosis y los intervalos de dosificación para estudios posteriores de QR 421a para su desarrollo clínico.
Traducción: Asociación Mácula Retina.
Web Relacionada