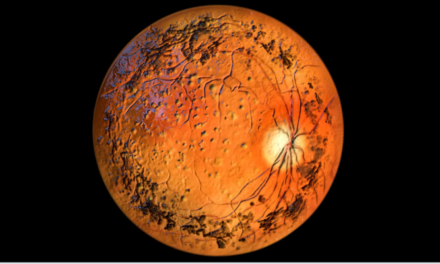
Investigadores utilizan células de pacientes para probar terapia génica para una forma de Amaurosis Congénita de Leber
Científicos del National Eye Institute (NEI) han desarrollado una prometedora técnica de terapia génica para una enfermedad rara que provoca una grave pérdida de visión en la infancia.
La enfermedad, una forma de amaurosis congénita de Leber, está causada por mutaciones autosómicas dominantes en el gen CRX, que son difíciles de tratar con terapia génica. Los científicos probaron su método utilizando tejidos de la retina fabricados en laboratorio a partir de células de pacientes, llamados organoides de la retina. Este método, que consiste en añadir copias del gen normal bajo el mecanismo de control nativo, restauró parcialmente la función del gen CRX. El informe del estudio aparece hoy en Stem Cell Reports. El NEI forma parte de los Institutos Nacionales de la Salud.
«Nuestro método de tratamiento, que añade más copias del gen normal, podría tratar potencialmente la Amaurosis congénita de Leber autosómica dominante causada por una variedad de mutaciones», dijo Anand Swaroop, PhD, jefe del Laboratorio de Neurobiología, Neurodegeneración y Reparación del NEI y autor principal del informe, en un comunicado de prensa del NEI.
La FDA aprobó Luxturna en 2017 para el tratamiento de pacientes con Amaurosis congénita de Leber con mutaciones en un gen llamado RPE65. Aunque fue aclamado como un gran avance en la terapia génica, Luxturna es ineficaz contra otras formas de LCA, incluidas las causadas por mutaciones autosómicas dominantes en el gen CRX.
El gen CRX codifica una proteína (también llamada CRX) que se une al ADN y da instrucciones a los fotorreceptores de la retina para que fabriquen pigmentos sensibles a la luz llamados opsinas. Sin la proteína CRX funcional, los fotorreceptores pierden su capacidad de detectar la luz y acaban muriendo.
Los trastornos como la LCA autosómico-dominante son difíciles de tratar con terapia génica, porque añadir más del gen normal no siempre restablece la función. Las personas con mutaciones autosómicas dominantes siguen teniendo una copia normal del gen, pero la versión mutante de la proteína interfiere con la proteína normal. A veces, en lugar de restablecer la función normal, la simple adición de más proteína normal puede potenciar la enfermedad de forma imprevisible.
Para explorar cómo la amplificación genética -añadir copias del gen normal- afectaría a la LCA autosómica dominante, el equipo de Swaroop desarrolló organoides de retina a partir de dos voluntarios con LCA y de sus familiares no afectados. Dirigidos por el doctor Kamil Kruczek, becario postdoctoral del laboratorio de Swaroop, construyeron los complejos tejidos similares a la retina en varias etapas, empezando por las células de la piel, induciendo la producción de fotorreceptores maduros y otras células de la retina con el perfil genético de cada voluntario. Como era de esperar, los organoides de los pacientes producían mucha menos opsina sensible a la luz que los organoides fabricados a partir de familiares no afectados.
Para controlar cuidadosamente la cantidad de gen CRX que expresarían los fotorreceptores, el equipo rediseñó el promotor de CRX para que pudiera ser administrado con el gen CRX como parte de la terapia génica. En genética un promotor es una región de ADN que controla la iniciación de la transcripción de una determinada porción del ADN a ARN. Un promotor por lo tanto, promueve la transcripción de un gen. Los investigadores introdujeron el gen y el promotor diseñado en un virus que los transportó a los fotorreceptores organoides.
La estrategia de amplificación genética del equipo restauró la función de la proteína CRX en los organoides de ambos pacientes, impulsando la expresión de opsinas en ambos tipos de fotorreceptores: bastones y conos.
«El hecho de que esta estrategia funcionara para ambas mutaciones de CRX fue muy emocionante», dijo Swaroop. «La amplificación genética puede ser una terapia viable para el ACV causado por otras mutaciones autosómicas dominantes».
«Este estudio de prueba de concepto de terapia génica es el primer paso hacia un tratamiento potencial para una forma rara de LCA», dijo Brian Brooks, MD, director clínico del NEI y coautor del estudio. «Es un gran ejemplo de la ciencia del laboratorio a la práctica, cuando los investigadores de la ciencia básica y clínica colaboran».
El estudio actual fue financiado a través de los programas propios del NEI y del Instituto Nacional de Alergias y Enfermedades Infecciosas, ambos parte de los NIH. Las muestras de los pacientes se recogieron en el Centro Clínico de los NIH, con el número de ensayo clínico NCT01432847.
Investigadores utilizan células de pacientes para probar terapia génica para una forma de Amaurosis Congénita de Leber.
Traducción: Asociación Mácula Retina.
Web Relacionada