La compañía ha pedido a la FDA la autorización de MCO-010, un tratamiento que podría devolver visión a personas con RP sin importar su mutación genética.
La aprobación podría llegar en 2026
Nanoscope Therapeutics ha comenzado el proceso para que la Agencia de Medicamentos de EE. UU. (FDA) apruebe MCO-010, la primera terapia génica “agnóstica al gen” para tratar la retinosis pigmentaria (RP). La empresa prevé completar la solicitud a principios de 2026 y espera que el tratamiento pueda estar disponible ese mismo año.
Un tratamiento que no depende del gen mutado
La retinosis pigmentaria es una enfermedad hereditaria que puede deberse a mutaciones en más de 100 genes distintos, lo que ha complicado el desarrollo de terapias eficaces. MCO-010 representa un cambio de paradigma: actúa sin necesidad de identificar la mutación genética del paciente y podría beneficiar a cualquier persona con RP avanzada.
“Por primera vez, personas que estaban en camino hacia la ceguera total podrían tener una oportunidad real de recuperar visión”, ha afirmado Sulagna Bhattacharya, directora ejecutiva y cofundadora de Nanoscope.
Cómo funciona MCO-010
MCO-010 es una terapia optogenética que se administra con una sola inyección en el ojo, sin cirugía ni pruebas genéticas previas. Transforma células bipolares de la retina en células sensibles a la luz, compensando la pérdida de fotorreceptores y permitiendo que el cerebro vuelva a recibir señales visuales.
“Los resultados han superado nuestras expectativas tanto en el laboratorio como en los ensayos clínicos”, señaló el Dr. Samarendra Mohanty, presidente y cofundador de Nanoscope.
Resultados prometedores
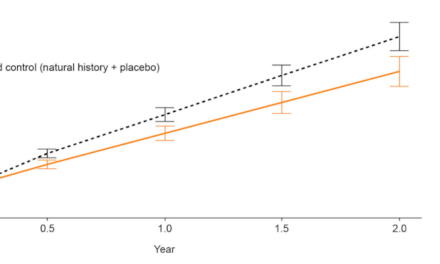
En el ensayo pivotal RESTORE (Fase 2b), MCO-010 mejoró de forma significativa la agudeza visual a las 52 semanas, con ganancias mantenidas durante tres años y sin efectos adversos graves. La terapia cuenta además con la designación de “vía rápida” de la FDA, lo que agiliza su revisión.
Una enfermedad que afecta a miles de personas
La RP es una de las principales causas de ceguera en adultos en edad laboral en EE. UU., donde afecta a más de 100.000 personas. Más de 25.000 ya han perdido gran parte de su visión.
“Con MCO-010 podríamos estar ante un cambio de paradigma”, afirma el Dr. Allen C. Ho, del Wills Eye Hospital. “Por primera vez, hay una esperanza real de mejorar la calidad de vida de estos pacientes”.
También en desarrollo para la enfermedad de Stargardt
Nanoscope trabaja además en ensayos con MCO-010 para tratar la enfermedad de Stargardt, y planea iniciar un ensayo de Fase 3 en 2025. La FDA ha concedido a MCO-010 las designaciones de “vía rápida” y “medicamento huérfano” tanto para la RP como para Stargardt.
Puedes consultar más información previa sobre MCO- en nuestra web:
Para consultar los ensayos clínicos que actualmente se están llevando a cabo con MCO, consultar: https://pubmed.ncbi.nlm.nih.gov/?term=mco-010