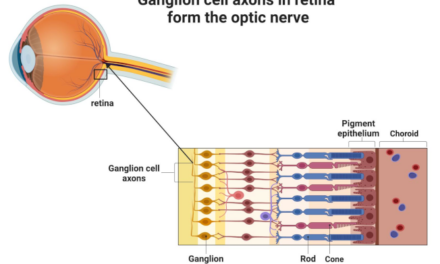
Apellis presenta los análisis funcionales de fase 3 de SYFOVRE (pegcetacoplan inyectable) para la atrofia geográfica (DMAE seca)
- Mostró beneficios visuales y calidad de vida mejorados en pacientes con lesiones extrafoveales
- Ralentizó la pérdida de células epiteliales pigmentarias y fotorreceptoras, ambas necesarias para la función visual
- Ocho resúmenes, incluyendo tres presentaciones orales, destacaron en la reunión anual de ARVO
Apellis Pharmaceuticals, Inc., una empresa biofarmacéutica global, comunicó el análisis post hoc de los estudios OAKS y DERBY de fase 3 de 24 meses evaluando SYFOVRE ™ (inyección de pegcetacoplan) para el tratamiento de la atrofia geográfica (AG) secundaria a la degeneración macular asociada con la edad (DMAE). Los análisis se informaron durante presentaciones orales en la Reunión Anual de la Asociación para la Investigación en Visión y Oftalmología (ARVO) que se llevó a cabo del 23 al 27 de abril en Nueva Orleans.
SYFOVRE mostró beneficios en la función visual y la calidad de vida en pacientes con lesiones extrafoveales (≥0,25 mm del centro foveal). Además, SYFOVRE mostró una reducción significativa en la pérdida de células fotorreceptoras y epiteliales pigmentarias de la retina (EPR), ambas necesarias para la visión. Estos análisis utilizaron datos de pacientes con imágenes de tomografía de coherencia óptica (OCT) SPECTRALIS®, que permitieron la segmentación automatizada basada en inteligencia artificial (IA) de las capas fotorreceptoras y EPR, así como la determinación de la cantidad de la región foveal central cubierta por la lesión de AG (ocupación foveal).
SYFOVRE mostró beneficios en la función visual y la calidad de vida en pacientes con lesiones extrafoveales
En el análisis de 24 meses, los pacientes tratados con SYFOVRE en comparación con el tratamiento simulado demostraron:
Preservación de 5,6 letras, equivalente a más de una línea de visión en un gráfico ETDRS, según lo medido por la agudeza visual mejor corregida (AVMC).
Un beneficio de 4,1 puntos en los resultados de calidad de vida relacionados con la visión, según lo medido por el NEI-VFQ-25. El cuestionario evalúa resultados, como la función social, la conducción y la dependencia de otros. Cuatro puntos se consideran clínicamente significativos. 1
«La pérdida de visión causada por AG puede afectar profundamente la independencia y el bienestar de una persona, por lo que es vital que SYFOVRE haya demostrado una pérdida de visión más lenta y una mejor calidad de vida en comparación con el tratamiento simulado en este análisis post hoc. Estos datos también respaldan el tratamiento anterior con SYFOVRE”, dijo Allen Chiang, MD, autor principal y profesor asociado de oftalmología en Wills Eye Hospital, Mid Atlantic Retina y Thomas Jefferson University. «Como el primer y único medicamento aprobado para AG, SYFOVRE representa una nueva era de tratamiento para esta enfermedad devastadora».
Debido a consideraciones de tamaño de muestra, los datos bimensuales y mensuales de OAKS y DERBY se combinaron para los grupos SYFOVRE (n = 131) y tratamiento simulado (n = 61). Estos datos se suman a los resultados de beneficios funcionales informados anteriormente en el análisis post hoc de microperimetría de la zona de unión.
SYFOVRE ralentizó la pérdida de células fotorreceptoras y EPR en comparación con el placebo
En el análisis de 24 meses de OAKS (n = 456) y DERBY (n = 435), SYFOVRE demostró una reducción significativa en la pérdida de células fotorreceptoras y EPR en comparación con el tratamiento simulado (todos los valores p nominales):
Células fotorreceptoras
Bimensual: 46% (OAKS; p <0,0001) y 46% (DERBY; p <0,0001)
Mensual: 53% (OAKS; p <0,0001) y 47% (DERBY; p <0,0001)
Células EPR
Bimensual: 20% (OAKS; p = 0,0002) y 21% (DERBY; p = 0,0005)
Mensual: 22% (OAKS; p = 0,0002) y 27% (DERBY; p <0,0001)
Las células EPR mantienen la integridad de las células fotorreceptoras, y ambos tipos de células son necesarios para la visión. Los datos fueron consistentes al comparar los ojos de estudio tratados con SYFOVRE con los ojos no tratados.
«Estamos orgullosos de compartir estos datos como parte de nuestras ocho presentaciones en la reunión de ARVO de este año, que muestran nuestro liderazgo en Atrofia Geográfica y retina», dijo Caroline Baumal, M.D., directora médica de Apellis. «SYFOVRE es un cambio de juego para la AG como el primer y único tratamiento para esta enfermedad implacable, y esperamos explorar su potencial para tratar otras enfermedades de la retina impulsadas por el complemento con necesidades significativas no satisfechas».
Las solicitudes de comercialización están actualmente bajo revisión con cinco agencias reguladoras en todo el mundo. Se espera una decisión en la UE a principios de 2024, y se esperan decisiones en Canadá, Australia, Suiza y el Reino Unido en la primera mitad de 2024.
Las presentaciones estarán disponibles en la página «Eventos y presentaciones» de la sección «Inversores y medios» del sitio web de la compañía.
Acerca de la metodología de función visual
El análisis de la función visual tiene en cuenta los predictores clave de pérdida de visión, incluida la distancia a la fóvea (≥0,25 mm desde el centro foveal) y la ocupación foveal. El análisis se ajustó por desequilibrios basales en las características de la enfermedad, incluida la ocupación foveal.
Acerca de los estudios OAKS y DERBY de Fase 3
OAKS (n = 637) y DERBY (n = 621) son estudios de Fase 3, multicéntricos, aleatorios, doble ciego y controlados con tratamiento simulado que comparan la eficacia y seguridad de SYFOVRE ™ (inyección de pegcetacoplan) con inyecciones simuladas en una población amplia y heterogénea de pacientes con atrofia geográfica (AG) secundaria a degeneración macular relacionada con la edad (DMAE). Los estudios evaluaron la eficacia de SYFOVRE mensual y cada dos meses en pacientes con atrofia geográfica (AG) evaluados por cambios en el área total de lesiones de atrofia geográfica (AG) desde el inicio, medidos por autofluorescencia del fondo.
En los estudios de Fase 3 a los 24 meses, tanto SYFOVRE cada dos meses como mensual redujeron el crecimiento de las lesiones de atrofia geográfica (AG) con efectos crecientes con el tiempo y mostraron un perfil de seguridad bien demostrado.
Acerca de la atrofia geográfica (AG)
La atrofia geográfica (AG) es una forma avanzada de degeneración macular relacionada con la edad y una de las principales causas de ceguera en todo el mundo, que afecta a más de un millón de estadounidenses y cinco millones de personas en todo el mundo. Es una enfermedad progresiva e irreversible causada por el crecimiento de lesiones que destruyen las células retinianas responsables de la visión. La pérdida de visión causada por la atrofia geográfica (AG) afecta gravemente la independencia y la calidad de vida al dificultar la participación en actividades diarias. En promedio, solo se necesitan 2.5 años para que las lesiones de atrofia geográfica (AG) comiencen a afectar la fóvea, que es responsable de la visión central.
Acerca de SYFOVRE ™ (inyección de pegcetacoplan)
SYFOVRE ™ (inyección de pegcetacoplan) es la primera y única terapia aprobada para la atrofia geográfica (GA). Al dirigirse a C3, SYFOVRE está diseñado para proporcionar un control integral del sistema complementario, parte del sistema inmunológico del cuerpo. SYFOVRE está aprobado en los Estados Unidos para el tratamiento de GA secundaria a degeneración macular relacionada con la edad.
Información importante sobre seguridad en EE. UU. para SYFOVRE ™ (inyección de pegcetacoplan)
CONTRAINDICACIONES
- SYFOVRE está contraindicado en pacientes con infecciones oculares o perioculares, y en pacientes con inflamación intraocular activa.
ADVERTENCIAS Y PRECAUCIONES
- Endoftalmitis y desprendimientos de retina. Las inyecciones intravítreas, incluyendo aquellas con SYFOVRE, pueden estar asociadas con endoftalmitis y desprendimientos de retina. Siempre se debe utilizar una técnica de inyección aséptica adecuada al administrar SYFOVRE para minimizar el riesgo de endoftalmitis. Se debe instruir a los pacientes para que informen cualquier síntoma sugestivo de endoftalmitis o desprendimiento de retina sin demora y se deben manejar adecuadamente.
- DMAE neovascular. En los ensayos clínicos, el uso de SYFOVRE se asoció con tasas aumentadas de DMAE neovascular (húmeda) o neovascularización coroidea (12% cuando se administró mensualmente, 7% cuando se administró cada dos meses y 3% en el grupo de control) para el mes 24. Los pacientes que reciben SYFOVRE deben ser monitoreados por signos de DMAE neovascular. En caso de que se requiera anti-factor de crecimiento endotelial vascular (anti-VEGF), debe administrarse por separado de la administración de SYFOVRE.
- Inflamación intraocular. En los ensayos clínicos, el uso de SYFOVRE se asoció con episodios de inflamación intraocular, incluyendo: vitritis, células vítreas, iridociclitis, uveítis, células de la cámara anterior, iritis y flare de la cámara anterior. Después de que la inflamación se resuelva, los pacientes pueden reanudar el tratamiento con SYFOVRE.
- Aumento de la presión intraocular. Un aumento agudo en la PIO puede ocurrir dentro de los minutos posteriores a cualquier inyección intravítrea, incluida SYFOVRE. La perfusión del disco óptico debe monitorearse después de la inyección y manejarse según sea necesario.
REACCIONES ADVERSAS
Las reacciones adversas más comunes (incidencia ≥5%) son molestias oculares, DMAE neovascular relacionada con la edad, moscas volantes vítreas y hemorragia conjuntival.
Análisis de fase 3 de SYFOVRE (pegcetacoplan inyectable) para la atrofia geográfica (DMAE seca)
Traducción: Asociación Mácula Retina
Fuente