Innovaciones quirúrgicas para tratar enfermedades médicas de la retina
Varios avances que están siendo sometidos a ensayos clínicos tienen como finalidad cambiar la manera en que se atiende a los pacientes.
El principal criterio de tratamiento de las enfermedades de la retina, en particular de la DMAE húmeda, ha variado entre el tratamiento médico (tratamiento con láser en la consulta, inyecciones y terapias tópicas) y el tratamiento quirúrgico (extirpación de la membrana neovascular coroidea subretiniana, translocación macular y trasplante quirúrgico del epitelio pigmentario de la retina [EPR]). La introducción de la terapia anti-VEGF dejó de lado el tratamiento quirúrgico de la DMAE húmeda 1. El uso ampliamente adoptado de bevacizumab intravítreo (Avastin, Genentech) impulsó el tratamiento de la DMAE húmeda en el ámbito médico 2.
En la retinopatía diabética (RD) se está produciendo una tendencia de tratamiento similar, con un cambio de la corrección quirúrgica primaria de las complicaciones proliferativas de la RD, como la hemorragia vítrea y los desprendimientos de retina traccionales, hacia la prevención de estas complicaciones por completo mediante terapias anti-VEGF.
PANORAMA es un ensayo clínico de fase 3 que evalúa a pacientes con RD no proliferativa de moderada a grave sin edema macular diabético con afectación central tratados con dosis de carga de aflibercept (Eylea, Regeneron) seguidas de inyecciones a intervalos fijos o inyecciones simuladas. En los años 1 y 2, menos pacientes en los brazos de aflibercept desarrollaron una complicación que amenazara la visión debido a la RD proliferativa, incluyendo la hemorragia vítrea y los desprendimientos de retina tracionales, cualquiera de los cuales requeriría una intervención quirúrgica.3,4
Entre las posibles terapias intravítreas anti-VEGF en fase 2 y 3 se encuentran faricimab (Genentech/Roche), conbercept (Chengdu Kanghong Biotech), OPT-302 (Opthea), KSI-301 (Kodiak) y GB-102 (Graybug Vision).5-20 Muchas de ellas prometen una mayor duración o una liberación sostenida para el tratamiento de la DMAE neovascular y la RD.
DMAE húmeda INNOVACIONES QUIRÚRGICAS
La cartera de productos médicos para la retina es potente, pero también lo es la cartera de productos quirúrgicos, y ya está resultando fructífera. En octubre, la FDA aprobó el sistema de administración por puerto con ranibizumab (Susvimo, Genentech/Roche), ampliando nuestro arsenal clínico para la DMAE húmeda. Hay otras innovaciones en el horizonte que pueden revolucionar el tratamiento de las enfermedades de la retina, y muchas de ellas aprovechan el poder de la terapia génica para proporcionar una dosis ininterrumpida de medicamentos.
La cirugía de la retina ha cambiado drásticamente desde el primer número de Retina Today. En 2006, los cirujanos aún debatían acaloradamente la utilidad de la cirugía con calibre de 25, y algunos concluían que el tiempo que se ahorraba con la técnica sin sutura se perdía debido al mayor tiempo de la cirugía1,2.
El trasplante autólogo de epitelio pigmentario de la retina seguía siendo una opción de tratamiento para muchos pacientes con DMAE, y los conferenciantes de las reuniones seguían tratando de averiguar cuándo era apropiado renunciar a la terapia anti-VEGF en favor de la probada extirpación quirúrgica subretiniana de las membranas neovasculares3,4.
Ah, ¿y ese telescopio miniatura implantable (SING IMT, Samsara) que ya está en su segunda generación?5 El Panel Asesor de Dispositivos Oftálmicos de la FDA sugirió que «no era aprobable» en julio de 2006 6 Referencias
1. Wimpissinger B, Kellner L, Stolba U, Binder S. Miniaturized instruments in vitreoretinal surgery: the future? Retina Today. 2006;1(2). 2. Eckardt C. 23-gauge surgery replaces 20- or 25-gauge — in most cases. Retina Today. 2006;1(4). 3. Kokame GT. An indication for surgery in the antiangiogenic era. Retina Today. 2006;1(2). 4. MacLaren RE. Autologous transplantation of rpe for the management of acute exudative AMD. Retina Today. 2006;1(2). 5. Samsara Vision: patients blinded by macular degeneration may benefit from implant technology [press release]. May 25, 2021. 6. Koury CB. Implantable telescope not recommended for approval, but there is reason for optimism. Retina Today. 2006;1(4).
El RGX-314 (Regenxbio) es un nuevo vector de virus adeno-asociado de serotipo 8 que se utiliza para administrar un gen que codifica un fragmento de unión a antígenos anti-VEGF. Está diseñado para producir una terapia continua de anti-VEGF para tratar la DMAE húmeda y la RD 21-23. La administración subretiniana de esta terapia requiere una vitrectomía pars plana (PPV) seguida de la creación de una ampolla subretiniana utilizando una aguja G 41 (Imagen)21,24.
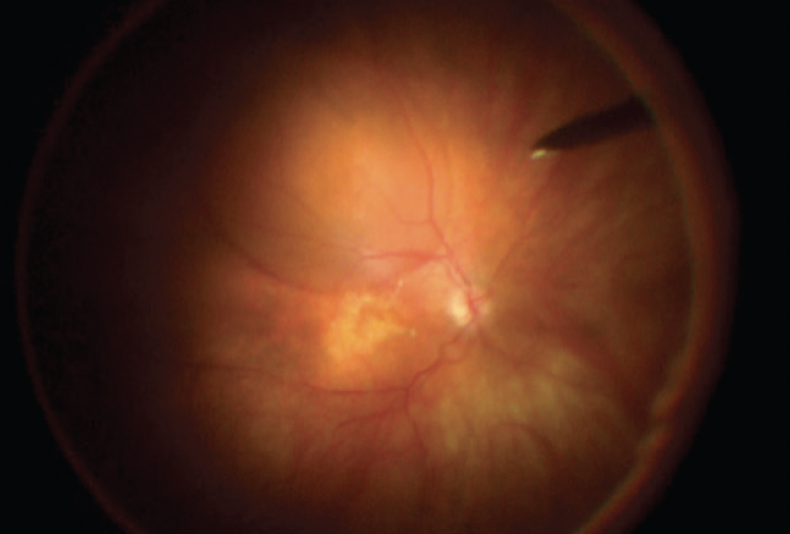
Imagen. Una ampolla subretiniana de RGX-314. Imagen por cortesía de Jeffrey S. Heier, MD
El ensayo clínico de fase 1/2a en pacientes con DMAE húmeda se ha completado con datos de 2 años de las cinco cohortes de dosis. Los pacientes de las cohortes 3, 4 y 5 mostraron una mejora de la visión y una reducción significativa de la necesidad de inyecciones suplementarias de anti-VEGF. Los niveles de proteína anti-VEGF dependieron de la dosis y se mantuvieron al menos durante 2 años 21,24. Los seis pacientes de la cohorte 3 se inscribieron en el estudio de seguimiento a largo plazo, y el efecto del tratamiento se demostró a lo largo de 3 años con una mejora media de la AVMC de +12 letras desde el inicio. La cohorte 3 mostró una disminución del 66,7% en la tasa de inyecciones anuales de anti-VEGF en comparación con los 12 meses anteriores al tratamiento con RGX-314. Las cohortes 4 y 5 mostraron una reducción del 58,3% y del 81,2% de las inyecciones de anti-VEGF, respectivamente, a 1,5 años. Ambas cohortes experimentaron una visión estable y una disminución del grosor de la retina24.
Cabe destacar que no se observaron reacciones inmunológicas, inflamación ocular relacionada con el fármaco ni inflamación posquirúrgica más allá de lo que se prevé tras una VPP rutinaria21. Sin embargo, los cambios pigmentarios de la retina en el 69% de los pacientes hicieron necesario un cambio en la técnica quirúrgica para ayudar a prevenir los cambios maculares21,25.
El ensayo de fase 2b/3 ATMOSPHERE está ahora reclutando y asignará aleatoriamente a 300 pacientes pseudofáquicos con DMAE húmeda para que reciban RGX-314 subretinal o ranibizumab intravítreo mensual. El criterio de valoración principal es el cambio en la agudeza visual en comparación con el ranibizumab mensual en la semana 54 26.
Volviendo al tratamiento médico, los ensayos de fase 2 AAVIATE y ALTITUTE están evaluando la inyección supracoroidal de RGX-314 en la consulta 22,23.
_1639674253.png)
Imagen. Estas imágenes del PDS demuestran un excelente cierre postoperatorio de la conjuntiva suprayacente (A) y un buen posicionamiento intraocular en la cámara vítrea (B).
El sistema de administración por puerto (PDS) con ranibizumab (Susvimo, Genentech/Roche) obtuvo la aprobación de la FDA en octubre1. El implante intraocular permanente y rellenable se rellena con la formulación concentrada en el quirófano y luego se implanta quirúrgicamente a través de una incisión en la pars plana (imagen). Los procedimientos de recambio posteriores se realizan en la clínica.
La aprobación se produce a raíz de los datos positivos del estudio de fase 3 ARCHWAY, en el que los pacientes con DMAE húmeda en el brazo de tratamiento con PDS lograron y mantuvieron ganancias de visión equivalentes a los que recibieron inyecciones mensuales de ranibizumab en las semanas 36 y 40 de tratamiento. En particular, el 98,4% de los pacientes del brazo de la PDS no necesitaron tratamiento suplementario hasta el primer recambio a las 24 semanas2.
PAGODA y PAVILION son ensayos aleatorios de fase 3 que evalúan la PDS con ranibizumab en el tratamiento de la retinopatía diabética3,4.
Referencias
1. FDA approves Genentech’s new treatment for wet age-related macular degeneration (AMD) [press release]. October 22, 2021. Accessed October 25, 2021. www.gene.com/media/news-features/fda-approves-genentech-s-new-treatment-for-wet-age-related-macular-degeneration-amd
2. Holekamp NM, Campochiaro PA, Chang M, et al; all Archway Investigators. Archway randomized phase 3 trial of the port delivery system with ranibizumab for neovascular age-related macular degeneration. Published online September 29, 2021. Ophthalmology.
3. A multicenter, randomized study in participants with diabetic retinopathy without center-involved diabetic macular edema to evaluate the efficacy, safety, and pharmacokinetics of ranibizumab delivered via the Port Delivery System relative to the comparator arm (PAVILION). Accessed August 26, 2021. clinicaltrials.gov/ct2/show/NCT04503551
4. A phase III, multicenter, randomized, visual assessor-masked, active-comparator study of the efficacy, safety, and pharmacokinetics of the Port Delivery System with ranibizumab in patients with diabetic macular edema (Pagoda). Accessed August 26, 2021. clinicaltrials.gov/ct2/show/NCT04108156
ATROFIA GEOGRÁFICA INNOVACIONES QUIRÚRGICAS
La atrofia geográfica (AG) es una enfermedad para la que una intervención quirúrgica eficiente podría tener un mayor impacto. Las futuras terapias quirúrgicas para la AG se basarán en la detección precoz, seguida de una terapia génica para frenar la progresión de la AG o de una terapia celular para reemplazar las células dañadas del EPR.
En los ensayos clínicos de fase 2 HORIZON y EXPLORE, GT005 (Gyroscope Therapeutics) se inyecta quirúrgicamente en el espacio subretiniano mediante un abordaje pars plana27,28.
GT005 es un vector de virus adeno-asociado diseñado para administrar un gen que codifica el factor I del complemento.27-29 El estudio FOCUS de fase 1/2 es un estudio de seguridad y búsqueda de dosis en el que GT005 se administra por vía subretiniana mediante un abordaje transvítreo (cohortes 1-4) o mediante el Orbit Subretinal Delivery Device System (Gyroscope Therapeutics), en el que GT005 se administra mediante canulación supracoroidal (cohortes 5-7) 29. Los datos provisionales mostraron que GT005 fue bien tolerado en todas las dosis y que el tratamiento produjo un aumento sostenido de los niveles del factor I del complemento vítreo en la mayoría de los pacientes.30 No se han producido acontecimientos inflamatorios oculares clínicamente significativos relacionados con GT005 30.
Un ensayo clínico de fase 1/2a en el Instituto Nacional del Ojo está evaluando la viabilidad del trasplante subretiniano de EPR derivado de células madre pluripotentes inducidas 31. Las células madre pluripotentes inducidas se generan a partir de las células somáticas de un paciente con AG, se diferencian en células de EPR y se cultivan en una monocapa que contiene un soporte biodegradable de ácido poliláctico-co-glicólico. A continuación, las células se trasplantan en el espacio subretiniano del mismo paciente con el objetivo de rescatar la retina neurosensorial suprayacente de una mayor degradación 31-33. Se requiere una VPP, y el trasplante se coloca a través de una retinotomía planificada, que requiere un taponamiento con gas 31.
OpRegen (Lineage Cell Therapeutics) utiliza células del EPR derivadas de células madre embrionarias humanas que se trasplantan por vía subretiniana en pacientes con AG. El ensayo de fase 1/2a incluye cuatro cohortes, las tres primeras de las cuales están completas. Los datos muestran que el tratamiento fue bien tolerado, sin acontecimientos adversos inesperados ni eventos inflamatorios. A los 15 meses, los ojos tratados presentaban una mejora estadísticamente significativa de la AVC en comparación con los ojos contrarios. Las primeras imágenes de OCT sugieren la posible resolución de la atrofia incompleta del EPR y de la retina externa tras el tratamiento34.
REFLEXIONES FINALES
Inevitablemente, el tratamiento básico de las enfermedades de la retina seguirá fluctuando entre las intervenciones médicas y quirúrgicas a medida que surjan nuevos planteamientos. Tenemos en el horizonte un arsenal de terapias, muchas de las cuales son quirúrgicas, que pueden proporcionar una mayor duración de la terapia y quizás incluso soluciones permanentes a estas complejas enfermedades.
Referencias
1. Gragoudas ES, Adamis AP, Cunningham ET, Feinsod M, Guyer DR; VEGF Inhibition Study in Ocular Neovascularization Clinical Trial Group. Pegaptanib for neovascular age-related macular de-generation. N Engl J Med. 2004;351(27):2805-2816. 2. Michels S, Rosenfeld PJ, Puliafito CA, Marcus EN, Venkatraman AS. Systemic bevacizumab (Avastin) therapy for neovascular age-related macular degeneration twelve-week results of an uncontrolled open-label clinical study. Ophthalmology. 2005;112(6):1035-1047. 3. Boyer DS. Treatment of moderately severe to severe nonproliferative diabetic retinopathy with intravitreal aflibercept injection: 52-week results from the phase 3 PANORAMA study. Invest Ophthalmol Vis Sci. 2019;60(9):1731-1731. 4. Lim JI. Intravitreal aflibercept injection for nonproliferative diabetic retinopathy: year 2 results from the PANORAMA study. Invest Ophthalmol Vis Sci. 2020;61(7):1381-1381. 5. A phase III, multicenter, randomized, double-masked, active comparator-controlled study to evaluate the efficacy and safety of faricimab (RO6867461) in patients with diabetic macular edema (YOSEMITE). Accessed August 9, 2021. clinicaltrials.gov/ct2/show/NCT03622580 6. A phase III, multicenter, randomized, double-masked, active comparator-controlled study to evaluate the efficacy and safety of faricimab (RO6867461) in patients with diabetic macular edema (RHINE). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03622593 7. A phase III, multicenter, randomized, double-masked, active comparator-controlled study to evaluate the efficacy and safety of faricimab in patients with neovascular age-related macular degeneration (TENAYA). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03823287 8. A phase III, multicenter, randomized, double-masked, active comparator-controlled study to evaluate the efficacy and safety of faricimab in patients with neovascular age-related macular degeneration (LUCERNE). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03823300 9. Safety and efficacy study of conbercept in diabetic macular edema (DME) (Sailing). Accessed July 17, 2021. clinicaltrials.gov/ct2/show/NCT02194634 10. A multicenter, double-masked, randomized, dose-ranging trial to evaluate the efficacy and safety of conbercept intravitreal injection in subjects with neovascular age-related macular degeneration (AMD) (PANDA-1). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03577899 11. A multicenter, double-masked, randomized, dose-ranging trial to evaluate the efficacy and safety of conbercept intravitreal injection in subjects with neovascular age-related macular degeneration (AMD) (PANDA-2). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03630952 12. A phase 3, multicentre, double-masked, randomised study to evaluate the efficacy and safety of intravitreal opt-302 in combination with ranibizumab, compared with ranibizumab alone, in participants with NAMD. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04757610 13. A phase 3, multicentre, double-masked, randomised study to evaluate the efficacy and safety of intravitreal OPT-302 in combination with aflibercept, compared with aflibercept alone, in participants with NAMD. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04757636 14. Phase 1b/2a study of OPT-302 in combination with aflibercept for persistent central-involved diabetic macular edema. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03397264 15. A phase 2b/3, prospective, randomized, double-masked, active comparator-controlled, multi-center study to investigate the efficacy and safety of repeated intravitreal administration of KSI-301 in subjects with neovascular (wet) age-related macular degeneration. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04049266 16. A prospective, randomized, double-masked, active comparator-controlled, multi-center, two-arm, phase 3 study to evaluate the efficacy and safety of intravitreal KSI-301 compared with intravitreal aflibercept in participants with visual impairment secondary to treatment-naïve diabetic macular edema (DME). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04611152 17. A prospective, randomized, double-masked, active comparator-controlled, multi-center, two-arm, phase 3 study to evaluate the efficacy and safety of intravitreal KSI-301 compared with intravitreal aflibercept in participants with visual impairment secondary to treatment-naïve diabetic macular edema (DME). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04603937 18. A phase 2a multicenter study evaluating the safety, tolerability, and pharmacodynamics of sunitinib malate depot formulation (GB-102) in subjects with diabetic macular edema (DME) and retinal vein occlusion (RVO). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04085341 19. A phase 1/2 multicenter study evaluating the safety, tolerability, and efficacy of an intravitreal depot formulation of sunitinib malate (GB-102) in subjects with neovascular age-related macular degeneration. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03249740 20. A phase 2b multicenter dose-ranging study evaluating the safety and efficacy of sunitinib malate depot formulation (GB-102) compared to aflibercept in subjects with neovascular (wet) age-related macular degeneration (ALTISSIMO Study). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03953079 21. Avery RL. Two year results from the subretinal RGX-314 gene therapy phase 1/2a study for the treatment of nAMD, and an update on suprachoroidal trials. Presented at: AAO 2021; February 13, 2021; Virtual. 22. RGX-314 gene therapy administered in the suprachoroidal space for participants with neovascular age-related macular degeneration (nAMD) (AAVIATE). Accessed October 29, 2021. clinicaltrials.gov/ct2/show/NCT04514653. 23. RGX-314 gene therapy administered in the suprachoroidal space for participants with diabetic retinopathy (DR) without center involved-diabetic macular edema (CI-DME) (ALTITUDE). Accessed October 29, 2021. clinicaltrials.gov/ct2/show/NCT04567550 24. Regenxbio. Regenxbio announces additional positive interim phase I/IIa and long-term follow-up data of RGX-314 for the treatment of wet AMD [press release]. February 16, 2021. Accessed October 25, 2021. regenxbio.gcs-web.com/news-releases/news-release-details/regenxbio-announces-additional-positive-interim-phase-iiia-and 25. Ho A. Subretinal gene therapy for exudative AMD. Presented at: Hawaiian Eye; May 10, 2021; Virtual. 26. A randomized, partially masked, controlled, phase 2b/3 clinical study to evaluate the efficacy and safety of RGX-314 gene therapy in participants with nAMD (ATMOSPHERE). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04704921 27. HORIZON: a phase II, open-label, outcomes-assessor masked, multicentre, randomised, controlled study to evaluate the safety and efficacy of two doses of GT005 administered as a single subretinal injection in subjects with geographic atrophy secondary to age-related macular degeneration. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04566445 28. EXPLORE: a phase II, outcomes assessor-masked, multicentre, randomised study to evaluate the safety and efficacy of two doses of GT005 administered as a single subretinal injection in subjects with geographic atrophy secondary to age-related macular degeneration. Accessed August 26, 2021. clinicaltrials.gov/ct2/show/NCT04437368 29. FocuS: first in human study to evaluate the safety and efficacy of GT005 administered in subjects with dry AMD. Accessed September 6, 2021. clinicaltrials.gov/ct2/show/NCT03846193 30. Interim results from a first-in-human phase I/II gene therapy study (FOCUS) of GT005, an investigational AAV2 vector encoding complement factor I (CFI), in patients with geographic atrophy (GA) [press release]. Accessed November 9, 2021. gyroscopetx.com/wp-content/uploads/2021/09/FOCUS-Data-Retina-Society-2021-Presentation_FINAL.pdf 31. A phase I/IIa trial for autologous transplantation of induced pluripotent stem cell-derived retinal pigment epithelium for geographic atrophy associated with age-related macular degeneration. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04339764 32. Ohmine S, Dietz AB, Deeds MC, et al. Induced pluripotent stem cells from GMP-grade hematopoietic progenitor cells and mononuclear myeloid cells. Stem Cell Res Ther. 2011;2(6):46. 33. Buchholz DE, Hikita ST, Rowland TJ, et al. Derivation of functional retinal pigmented epithelium from induced pluripotent stem cells. Stem Cells. 2009;27(10):2427-2434. 34. Ip M. OpRegen trial: phase I/IIa dose escalation study of human embryonic stem cell–derived retinal pigment epithelium cells transplanted subretinally in patients with advanced AMD. Presented at AAO 2021; November 12, 2021; New Orleans, LA
1. Gragoudas ES, Adamis AP, Cunningham ET, Feinsod M, Guyer DR; VEGF Inhibition Study in Ocular Neovascularization Clinical Trial Group. Pegaptanib for neovascular age-related macular de-generation. N Engl J Med. 2004;351(27):2805-2816. 2. Michels S, Rosenfeld PJ, Puliafito CA, Marcus EN, Venkatraman AS. Systemic bevacizumab (Avastin) therapy for neovascular age-related macular degeneration twelve-week results of an uncontrolled open-label clinical study. Ophthalmology. 2005;112(6):1035-1047. 3. Boyer DS. Treatment of moderately severe to severe nonproliferative diabetic retinopathy with intravitreal aflibercept injection: 52-week results from the phase 3 PANORAMA study. Invest Ophthalmol Vis Sci. 2019;60(9):1731-1731. 4. Lim JI. Intravitreal aflibercept injection for nonproliferative diabetic retinopathy: year 2 results from the PANORAMA study. Invest Ophthalmol Vis Sci. 2020;61(7):1381-1381. 5. A phase III, multicenter, randomized, double-masked, active comparator-controlled study to evaluate the efficacy and safety of faricimab (RO6867461) in patients with diabetic macular edema (YOSEMITE). Accessed August 9, 2021. clinicaltrials.gov/ct2/show/NCT03622580 6. A phase III, multicenter, randomized, double-masked, active comparator-controlled study to evaluate the efficacy and safety of faricimab (RO6867461) in patients with diabetic macular edema (RHINE). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03622593 7. A phase III, multicenter, randomized, double-masked, active comparator-controlled study to evaluate the efficacy and safety of faricimab in patients with neovascular age-related macular degeneration (TENAYA). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03823287 8. A phase III, multicenter, randomized, double-masked, active comparator-controlled study to evaluate the efficacy and safety of faricimab in patients with neovascular age-related macular degeneration (LUCERNE). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03823300 9. Safety and efficacy study of conbercept in diabetic macular edema (DME) (Sailing). Accessed July 17, 2021. clinicaltrials.gov/ct2/show/NCT02194634 10. A multicenter, double-masked, randomized, dose-ranging trial to evaluate the efficacy and safety of conbercept intravitreal injection in subjects with neovascular age-related macular degeneration (AMD) (PANDA-1). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03577899 11. A multicenter, double-masked, randomized, dose-ranging trial to evaluate the efficacy and safety of conbercept intravitreal injection in subjects with neovascular age-related macular degeneration (AMD) (PANDA-2). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03630952 12. A phase 3, multicentre, double-masked, randomised study to evaluate the efficacy and safety of intravitreal opt-302 in combination with ranibizumab, compared with ranibizumab alone, in participants with NAMD. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04757610 13. A phase 3, multicentre, double-masked, randomised study to evaluate the efficacy and safety of intravitreal OPT-302 in combination with aflibercept, compared with aflibercept alone, in participants with NAMD. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04757636 14. Phase 1b/2a study of OPT-302 in combination with aflibercept for persistent central-involved diabetic macular edema. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03397264 15. A phase 2b/3, prospective, randomized, double-masked, active comparator-controlled, multi-center study to investigate the efficacy and safety of repeated intravitreal administration of KSI-301 in subjects with neovascular (wet) age-related macular degeneration. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04049266 16. A prospective, randomized, double-masked, active comparator-controlled, multi-center, two-arm, phase 3 study to evaluate the efficacy and safety of intravitreal KSI-301 compared with intravitreal aflibercept in participants with visual impairment secondary to treatment-naïve diabetic macular edema (DME). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04611152 17. A prospective, randomized, double-masked, active comparator-controlled, multi-center, two-arm, phase 3 study to evaluate the efficacy and safety of intravitreal KSI-301 compared with intravitreal aflibercept in participants with visual impairment secondary to treatment-naïve diabetic macular edema (DME). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04603937 18. A phase 2a multicenter study evaluating the safety, tolerability, and pharmacodynamics of sunitinib malate depot formulation (GB-102) in subjects with diabetic macular edema (DME) and retinal vein occlusion (RVO). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04085341 19. A phase 1/2 multicenter study evaluating the safety, tolerability, and efficacy of an intravitreal depot formulation of sunitinib malate (GB-102) in subjects with neovascular age-related macular degeneration. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03249740 20. A phase 2b multicenter dose-ranging study evaluating the safety and efficacy of sunitinib malate depot formulation (GB-102) compared to aflibercept in subjects with neovascular (wet) age-related macular degeneration (ALTISSIMO Study). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT03953079 21. Avery RL. Two year results from the subretinal RGX-314 gene therapy phase 1/2a study for the treatment of nAMD, and an update on suprachoroidal trials. Presented at: AAO 2021; February 13, 2021; Virtual. 22. RGX-314 gene therapy administered in the suprachoroidal space for participants with neovascular age-related macular degeneration (nAMD) (AAVIATE). Accessed October 29, 2021. clinicaltrials.gov/ct2/show/NCT04514653. 23. RGX-314 gene therapy administered in the suprachoroidal space for participants with diabetic retinopathy (DR) without center involved-diabetic macular edema (CI-DME) (ALTITUDE). Accessed October 29, 2021. clinicaltrials.gov/ct2/show/NCT04567550 24. Regenxbio. Regenxbio announces additional positive interim phase I/IIa and long-term follow-up data of RGX-314 for the treatment of wet AMD [press release]. February 16, 2021. Accessed October 25, 2021. regenxbio.gcs-web.com/news-releases/news-release-details/regenxbio-announces-additional-positive-interim-phase-iiia-and 25. Ho A. Subretinal gene therapy for exudative AMD. Presented at: Hawaiian Eye; May 10, 2021; Virtual. 26. A randomized, partially masked, controlled, phase 2b/3 clinical study to evaluate the efficacy and safety of RGX-314 gene therapy in participants with nAMD (ATMOSPHERE). Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04704921 27. HORIZON: a phase II, open-label, outcomes-assessor masked, multicentre, randomised, controlled study to evaluate the safety and efficacy of two doses of GT005 administered as a single subretinal injection in subjects with geographic atrophy secondary to age-related macular degeneration. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04566445 28. EXPLORE: a phase II, outcomes assessor-masked, multicentre, randomised study to evaluate the safety and efficacy of two doses of GT005 administered as a single subretinal injection in subjects with geographic atrophy secondary to age-related macular degeneration. Accessed August 26, 2021. clinicaltrials.gov/ct2/show/NCT04437368 29. FocuS: first in human study to evaluate the safety and efficacy of GT005 administered in subjects with dry AMD. Accessed September 6, 2021. clinicaltrials.gov/ct2/show/NCT03846193 30. Interim results from a first-in-human phase I/II gene therapy study (FOCUS) of GT005, an investigational AAV2 vector encoding complement factor I (CFI), in patients with geographic atrophy (GA) [press release]. Accessed November 9, 2021. gyroscopetx.com/wp-content/uploads/2021/09/FOCUS-Data-Retina-Society-2021-Presentation_FINAL.pdf 31. A phase I/IIa trial for autologous transplantation of induced pluripotent stem cell-derived retinal pigment epithelium for geographic atrophy associated with age-related macular degeneration. Accessed July 15, 2021. clinicaltrials.gov/ct2/show/NCT04339764 32. Ohmine S, Dietz AB, Deeds MC, et al. Induced pluripotent stem cells from GMP-grade hematopoietic progenitor cells and mononuclear myeloid cells. Stem Cell Res Ther. 2011;2(6):46. 33. Buchholz DE, Hikita ST, Rowland TJ, et al. Derivation of functional retinal pigmented epithelium from induced pluripotent stem cells. Stem Cells. 2009;27(10):2427-2434. 34. Ip M. OpRegen trial: phase I/IIa dose escalation study of human embryonic stem cell–derived retinal pigment epithelium cells transplanted subretinally in patients with advanced AMD. Presented at AAO 2021; November 12, 2021; New Orleans, LA
Autores: Jordan D. Deaner, MD; Lejla Vajzovic, MD.
Traducción: Asociación Mácula Retina
Web Relacionada




